Ревматоидный артрит (Rheumatoid Arthritis) -
аутоиммунное ревматическое заболевание, которое проявляется синовиитом, хроническим деструктивным артритом и системным поражением
 внутренних органов. Распространённость ревматоидного артрита (РА) среди взрослого населения составляет от 0,5% до 2% (у пожилых
женщин – около 5%). Пик начала заболевания – 40–55 лет, однако вовлекаются все возрастные группы, включая детей. Чаще болеют женщины,
и соотношение женщин к мужчинам составляет 2,5:1. Заболевание является полигенным и генетически гетерогенным, в частности наиболее
тесная ассоциация установлена для отдельной формы РА – анкилозирующего спондилоартрита (болезни Бехтерева) – HLA-B27. Среди факторов
окружающей среды значимыми являются гормональные факторы, персистентные инфекции, негативные профессиональные факторы, а также
особенности состава микробиоты макроорганизма. внутренних органов. Распространённость ревматоидного артрита (РА) среди взрослого населения составляет от 0,5% до 2% (у пожилых
женщин – около 5%). Пик начала заболевания – 40–55 лет, однако вовлекаются все возрастные группы, включая детей. Чаще болеют женщины,
и соотношение женщин к мужчинам составляет 2,5:1. Заболевание является полигенным и генетически гетерогенным, в частности наиболее
тесная ассоциация установлена для отдельной формы РА – анкилозирующего спондилоартрита (болезни Бехтерева) – HLA-B27. Среди факторов
окружающей среды значимыми являются гормональные факторы, персистентные инфекции, негативные профессиональные факторы, а также
особенности состава микробиоты макроорганизма.
Иммунопатогенез. Внутрисуставное воспаление – это результат взаимодействия между резидентными клетками
синовиальной оболочки (синовиоцитами), макрофагами, дендритными клетками, NK-клетками, нейтрофилами и эффекторными клетками
адаптивных иммунных ответов, которые являются источниками большого числа различных воспалительных медиаторов. Преобладающим
механизмом адаптивных иммунных ответов считается Th1-путь.
Неизвестный артритогенный эпитоп фагоцитируется макрофагами, распознаётся наивными CD4+ Т-клетками с
последующей клональной экспансией аутореактивных CD4+ Т-клеток (Th1, а также Th17), которые проникают в синовиальную оболочку,
где протекает эффекторная стадия аутоиммунного ответа по IV типу с активацией
антигенпредставляющих макрофагов и продукцией разных медиаторов
воспаления, включая провоспалительные цитокины (IL-2, IL-17, IL-18, IFN-γ, TNF-α, и др.). Локальное воспаление приводит
к повреждению синовиоцитов, миграции разных клеток и дальнейшему прогрессированию процесса. Привлеченные в сустав нейтрофилы,
макрофаги, а также резидентные дендритные клетки и остеокласты выделяют, наряду с провоспалительными цитокинами, активные метаболиты
кислорода, оксид азота, лизосомальные ферменты и металлопротеиназы, что приводит к разрушению хрящевой и костной ткани.
Количественный или качественный дефицит pТreg, часто выявляемый у больных РА, и другие иммунорегуляторные
дефекты вносят вклад в усиление воспалительно-деструктивных процессов.
В качестве индукторов В-клеточного ответа при РА могут выступать ДНК поврежденных клеток и другие
ядерные антигены, коллаген, агрегированный IgG, цитруллинированные протеины. Наибольшей специфичностью
обладают тесты на выявление антител к цитруллинированным протеинам (АЦЦП). Цитруллин – аминокислота,
которая образуется из аргинина в результате посттрансляционной модификации белков лизосомальными ферментами. У некоторых больных РА
обнаруживают антитела к агрегированному IgG – ревматоидный фактор (РФ). Этот тест всё ещё используют
в качестве одного из дополнительных диагностических критериев РА. С участием аутоантител реализуется иммунокомплексный механизм
иммунного воспаления (III тип), которое может затрагивать и другие органы и ткани (васкулит в
почках, легких, сердце, ЦНС), что является основой системных и комбинированных форм РА. Однако, описанные аутоантитела могут
присутствовать в высоких концентрациях у пациентов с другими аутоиммунными расстройствами, а также у пожилых людей. Предполагается,
что аутоиммунные процессы играют ведущую роль на ранних стадиях РА, на поздних стадиях большее значение имеют неиммунные механизмы,
а именно ремоделирование – разрастание фиброзной ткани и разрушение суставного хряща, что существенно
нарушает функцию вовлечённых суставов.
См. калькулятор расчёта активности ревматоидного артрита - индекса DAS28.
Клиническая картина. В зоне разрастания воспаленной синовиальной оболочки формируется грануляционная
ткань – паннус, состоящая из пролиферирующих фибробластов, мелких сосудов, лимфоцитов, макрофагов,
плазматических клеток. Паннус, являясь источником гидролитических ферментов и провоспалительных цитокинов, проникает в хрящ и
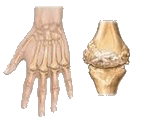
костную ткань, разрушает их. Первоначальными симптомами являются артралгии, чаще в области мелких суставов, нарушение подвижности
и утренняя скованность движений. В месте разрушений постепенно развивается анкилоз – заращение полости
сустава грануляционной тканью, что почти полностью нарушает функцию сустава. Хроническое воспаление околосуставных тканей, капсулы
суставов, связок, сухожилий могут приводить к деформации суставов, подвывихам, контрактурам. |
|
Лечение включает медикаментозную
болезнь-модифицирующую терапию: нестероидные противовоспалительные препараты, глюкокортикоиды, цитостатики.
В последние годы всё возрастающее место в терапии РА занимают биолоджики (моноклональные антитела), способные
связываться с провоспалительными цитокинами, их рецепторами, поверхностными молекулами В-клеток, лигандами для костимуляторных
молекул Т-клеток. Также используются ингибиторы сигналинга. |
 |



 внутренних органов. Распространённость ревматоидного артрита (РА) среди взрослого населения составляет от 0,5% до 2% (у пожилых
женщин – около 5%). Пик начала заболевания – 40–55 лет, однако вовлекаются все возрастные группы, включая детей. Чаще болеют женщины,
и соотношение женщин к мужчинам составляет 2,5:1. Заболевание является полигенным и генетически гетерогенным, в частности наиболее
тесная ассоциация установлена для отдельной формы РА – анкилозирующего спондилоартрита (болезни Бехтерева) – HLA-B27. Среди факторов
окружающей среды значимыми являются гормональные факторы, персистентные инфекции, негативные профессиональные факторы, а также
особенности состава микробиоты макроорганизма.
внутренних органов. Распространённость ревматоидного артрита (РА) среди взрослого населения составляет от 0,5% до 2% (у пожилых
женщин – около 5%). Пик начала заболевания – 40–55 лет, однако вовлекаются все возрастные группы, включая детей. Чаще болеют женщины,
и соотношение женщин к мужчинам составляет 2,5:1. Заболевание является полигенным и генетически гетерогенным, в частности наиболее
тесная ассоциация установлена для отдельной формы РА – анкилозирующего спондилоартрита (болезни Бехтерева) – HLA-B27. Среди факторов
окружающей среды значимыми являются гормональные факторы, персистентные инфекции, негативные профессиональные факторы, а также
особенности состава микробиоты макроорганизма.