Moноциты составляют примерно
4-8 % среди лейкоцитов крови. Они развиваются в костном мозге,
подразделяются на 1) классические (80-90%), 2) "патрульные" (5-10%) и 3) промежуточные (5-10%) моноциты.
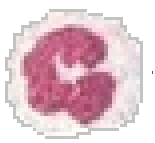 Классические моноциты циркулируют в кровотоке в течение нескольких часов,
"патрульные" - до недели. Все моноциты являются провоспалительными клетками, инфильтрирующими сайты воспаления,
способные мигрировать в ткани и превращаться в макрофаги и воспалительные дендритные клетки. Однако описаны макрофаги,
имеющие немоноцитарное происхождение. Клетки Лангерганса также имеют моноцитарное происхождение. Классические моноциты циркулируют в кровотоке в течение нескольких часов,
"патрульные" - до недели. Все моноциты являются провоспалительными клетками, инфильтрирующими сайты воспаления,
способные мигрировать в ткани и превращаться в макрофаги и воспалительные дендритные клетки. Однако описаны макрофаги,
имеющие немоноцитарное происхождение. Клетки Лангерганса также имеют моноцитарное происхождение.
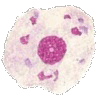
Макрофаги, открытые Нобелевским лауреатом (1908)
И.И. Мечниковым, играют важную роль в естественном иммунитете и
адаптивных иммунных ответах. Они могут фагоцитировать микробы,
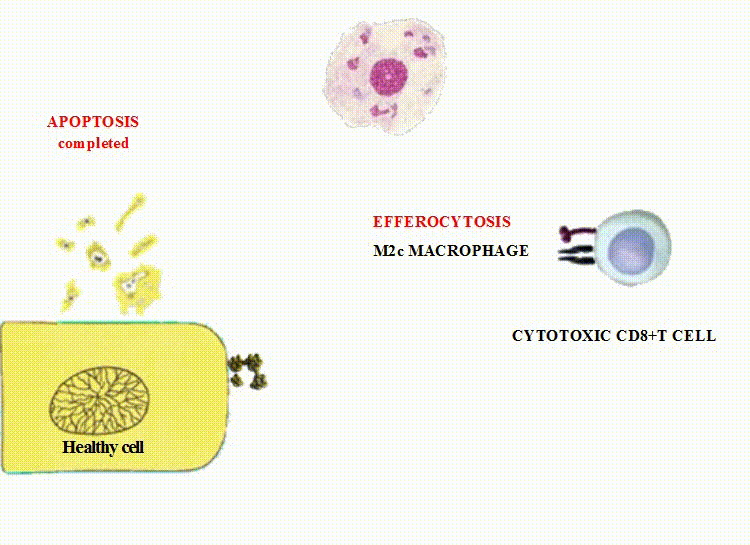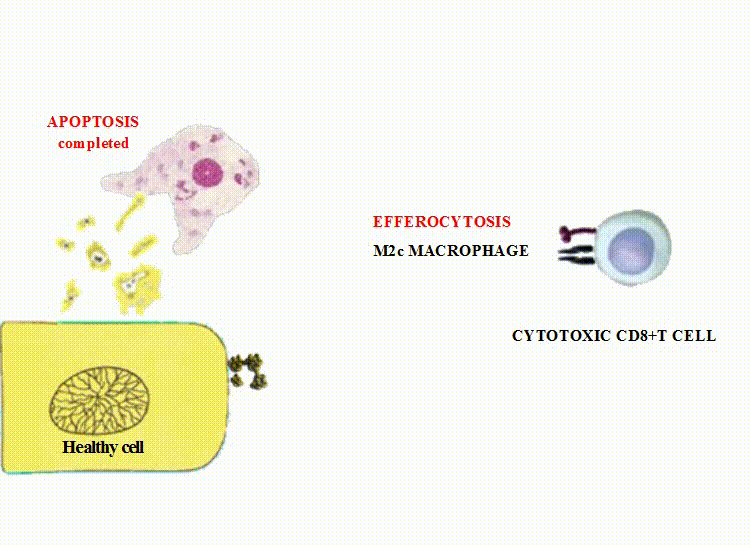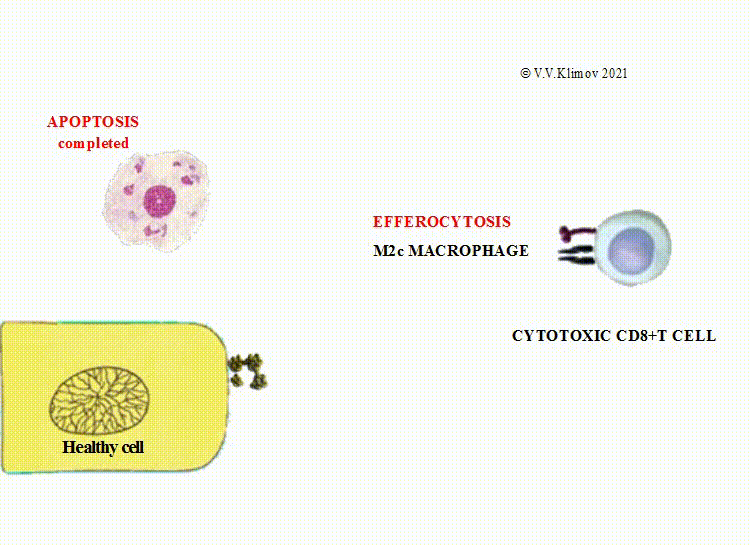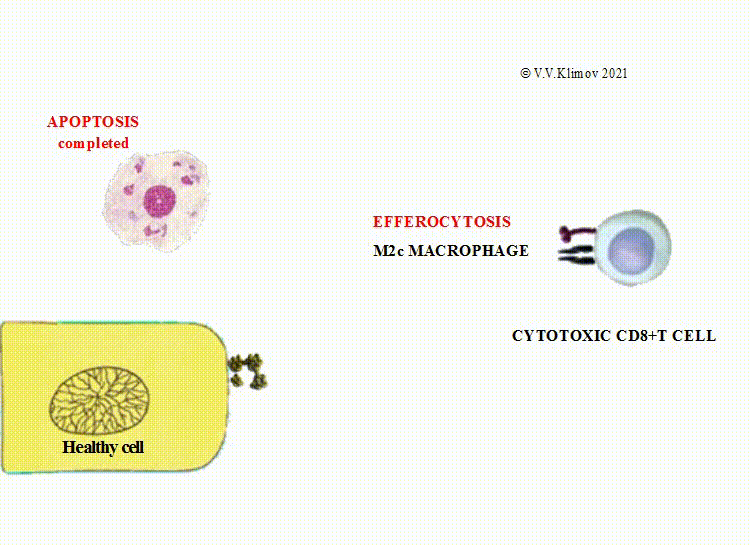
иммунные комплексы и производные клеток: апоптотические частицы и внеклеточные везикулы
(микровезикулы и экзосомы) путём эффероцитоза,
 захватывать, процессировать и представлять антигены Т-клеткам, а также секретировать многочисленные продукты:
цитокины и хемокины, белки комплемента, протеиназы, метаболиты арахидоновой кислоты, оксид азота
и другие кислородные радикалы, матричные металлопротеиназы (коллагеназа и др.). захватывать, процессировать и представлять антигены Т-клеткам, а также секретировать многочисленные продукты:
цитокины и хемокины, белки комплемента, протеиназы, метаболиты арахидоновой кислоты, оксид азота
и другие кислородные радикалы, матричные металлопротеиназы (коллагеназа и др.).
Макрофаги несут на себе ряд важных рецепторов, необходимых для связывания паттернов и липополисахаридов (ЛПС) - TLR
и CD14, комплемента - CR3 и CR4, Fc-фрагмента IgG - FcγRI (CD64), клеточные адгезивные молекулы. Например,
макрофагальный маркёр CD68 является одним из scavenger receptors ("рецепторов-мусорщиков").
Известны две основные популяции макрофагов: воспалительные (М1) и противовоспалительные (М2).
Воспалительные (М1) макрофаги вовлечены
в поляризацию Т-хелперов 1 (через секрецию IL-12), процессинг антигена,
CD4+T-клеточный ответ, иммунное воспаление (ГЗТ) и синтез
провоспалительных цитокинов: IL-1β, IL-6, TNF-α (ответственных, в том числе, за "цитокиновый шторм").
Активация М1 обеспечивается через IFN-γ, а инактивация - Тh2 (IL-10).
Противовоспалительные (М2) макрофаги вовлечёны в процессы поддержания
толерантности и регенерацию тканей. Но М2 могут стимулировать опухолевый рост. Поляризация в М2 фенотип осуществляется IL-4, IL-10 и IL-13.
М2 макрофаги являются очень гетерогенной популяцией, которая разделяется на четыре субпопуляции:
М2а (альтернативно-активированные макрофаги) обладают выраженными иммуносупрессивными
эффектами;
М2b (активированные макрофаги типа II) характеризуются амбивалентными свойствами;
M2c (деактивированные макрофаги) осуществляют клиренс мёртвых клеток и фрагментов клеток;
M2d (ассоциированные с опухолями макрофаги) (TAM) стимулируют рост раковых клеток.
Экстрацеллюлярные везикулы, подвергающиеся эффероцитозу М2 макрофагами, содержат сильные биоактивные субстанции,
являющиеся дополнительным стимулом для М2-поляризации.
|

Классические моноциты циркулируют в кровотоке в течение нескольких часов, "патрульные" - до недели. Все моноциты являются провоспалительными клетками, инфильтрирующими сайты воспаления, способные мигрировать в ткани и превращаться в макрофаги и воспалительные дендритные клетки. Однако описаны макрофаги, имеющие немоноцитарное происхождение. Клетки Лангерганса также имеют моноцитарное происхождение.
захватывать, процессировать и представлять антигены Т-клеткам, а также секретировать многочисленные продукты: цитокины и хемокины, белки комплемента, протеиназы, метаболиты арахидоновой кислоты, оксид азота и другие кислородные радикалы, матричные металлопротеиназы (коллагеназа и др.).